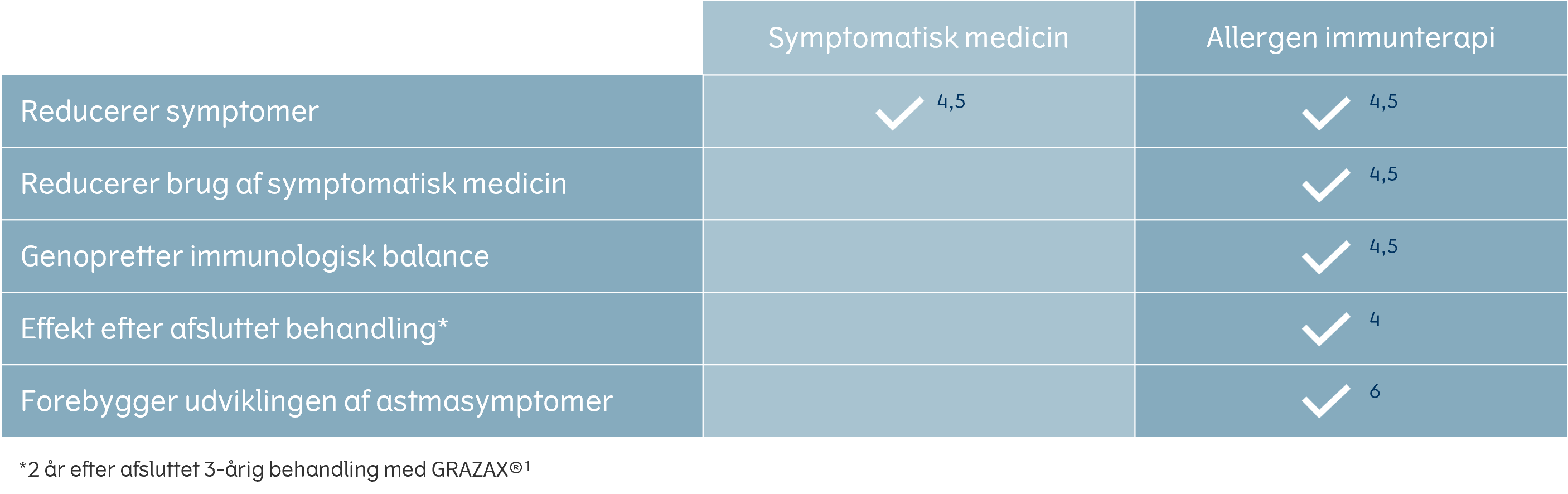
*Vs. placebo. Alle patienter havde adgang til symptomlindrende medicin.
**Dermatofagoider, pteronyssinus og dermatofagoider, farine.
¤Træpollen, græspollen, husstøvmider.
¤¤Se produktresuméerne for ACARIZAX®, GRAZAX® og ITULAZAX® for mere detaljeret information.1-3
§Aktuel symptomatisk allergisk rhinits og brug af symptomatisk medicin var forbundet med at miste en eller flere karakterer i matematik, engelsk eller naturvidenskabelige fag mellem vinter og sommer vs. studerende uden allergisk rhinitis-symptomer eller medicin.14-16
[1]Produktresume GRAZAX®
[2] Produktresume ACARIZAX®
[3] Produktresume ITULAZAX®
[4] Bousquet J et al. J Allergy Clin Immunol. 2020 Jan;145(1):70-80.
[5] Roberts G et al. Allergy. 2018 Apr;73(4):765-798.
[6] Alvaro-Lozano M et al. Pediatr Allergy Immunol. 2020 May;31 Suppl 25(Suppl 25):1-101.
[7] Global Initiative for Asthma (GINA) 2022 GINA Report V2
[8] Reich K et al. Clin Ther. 2011 Jul;33(7):828-40.
[9] Valovirta et al. Current Opinion in Allergy and Clinical Immunology 2008, 8:1–9
[10] Bousquet JB et al. Int Arch Allergy Immunol 2013;160:393–400
[11] Canonica et al. World Allergy Organization Journal 2014, 7:6. 17-25
[12] Bousquet J et al. Allergy. 2008: 63 (Suppl. 86): 8–160
[13] Romano MR et al. Allergy Asthma Clin Immunol. 2019 Dec 6:15:81
[14] de la Hoz Caballer B et al. Am J Rhinol Allergy. 2012 Sep-Oct;26(5):390-4.
[15] Blanc PD et al. J Clin Epidemiol. 2001 Jun;54(6):610-8.
[16] Walker S et al. J Allergy Clin Immunol. 2007 Aug;120(2):381-7.
[17] Sigurdardottir ST et al. Allergy. 2021 Sep;76(9):2855-2865.
[18] Scadding G and Walker. Prim Care Respir J. 2012 Jun;21(2):222-8
[19] Woehlk C et al. Ann Allergy Immunol. 2018;120:169-76.
ACARIZAX® DERMATOPHAGOIDES PTERONYSSINUS, DERMATOPHAGOIDES FARINAE. Standardiseret allergenekstrakt fra husstøvmider. Frysetørrede sublinguale tabletter 12 SQ-HDM. Indikation: Voksne patienter (18-65 år) diagnosticeret via klinisk anamnese og en positiv test for husstøvmidesensibilisering (hudpriktest og/eller specifik IgE) med mindst en af følgende tilstande:
- Vedvarende moderat til svær husstøvmideudløst allergisk rhinitis trods brug af symptomlindrende behandling.
- Husstøvmideudløst allergisk astma, som ikke er velkontrolleret ved inhalationscorticosteroider og forbundet med let til svær husstøvmideudløst allergisk rhinitis. Patientens astmastatus skal nøje vurderes, før behandlingen indledes.
Unge (12-17 år) diagnosticeret via klinisk anamnese og positiv test for husstøvmidesensibilisering (hudpriktest og/eller specifik IgE) med vedvarende moderat til svær husstøvmideudløst allergisk rhinitis trods brug af symptomlindrende behandling.
Dosering: Én frysetørret sublingual tablet dagligt. Den kliniske effekt kan forventes at sætte ind 8-14 uger efter initiering. Internationale retningslinjer henviser til en behandlingsperiode på 3 år for at opnå modifikation af sygdommen. Hvis der ikke observeres forbedring i løbet af det første års behandling, er der ingen indikation for at fortsætte behandlingen. Behandling skal initieres af læger med erfaring i behandling af allergiske sygdomme. Den første frysetørrede sublinguale tablet bør tages under lægeligt opsyn, og patienten bør overvåges i mindst en halv time, for at patient og læge kan få lejlighed til at diskutere evt. umiddelbare bivirkninger og mulige tiltag. Hvis behandlingen afbrydes i mere end 7 dage, anbefales det at kontakte en læge, før behandlingen genoptages. Kontraindikationer: Overfølsomhed over for hjælpestofferne. FEV1 < 70 % af den forventede værdi (efter tilstrækkelig farmakologisk behandling) ved initiering af behandlingen. Svær astmaeksacerbation inden for de seneste 3 måneder. Hos patienter med astma, som oplever en akut luftvejsinfektion, bør initiering af behandlingen udsættes, indtil infektionen er ovre. Aktiv eller dårligt kontrollerede autoimmune sygdomme, immundefekter, nedsat immunforsvar, immunosuppression og maligne neoplastiske sygdomme med aktuel sygdomsrelevans. Akut svær oral inflammation eller orale sår. Særlige advarsler og forsigtighedsregler: Ikke beregnet til behandling af akutte astmaeksacerbationer. I tilfælde af en akut astmaeksacerbation skal der bruges en korttidsvirkende bronkodilatator. Lægehjælp skal omgående søges, hvis patienternes astma pludselig forværres. Skal i starten bruges som supplerende behandling til allerede eksisterende astmalægemidler. Abrupt ophør med astmamedicin efter initiering af Acarizax anbefales ikke. Behandlingen skal seponeres, og en læge skal omgående kontaktes i tilfælde af svære systemiske allergiske reaktioner, svære astmaeksacerbationer, angioødem, synkebesvær, åndedrætsbesvær, stemmeforandringer, hypotension eller følelse af opfyldning i halsen. De indsættende systemiske symptomer kan omfatte rødmen, pruritus, varmefornemmelser, generelt ubehag og uro/angst. En mulig behandling af svære systemiske allergiske reaktioner er adrenalin. Patienter med hjertesygdomme kan være udsat for øget risiko i tilfælde af systemiske allergiske reaktioner. Initiering hos patienter, der tidligere har haft en systemisk allergisk reaktion over for subkutan husstøvmide-immunterapi, skal nøje overvejes, og der skal være foranstaltninger til rådighed til behandling af mulige reaktioner. Hos patienter med svær oral inflammation, orale sår eller efter oral kirurgi, herunder dental ekstraktion eller efter tab af tand, bør initiering af Acarizax udskydes, og igangværende behandling bør midlertidigt seponeres for at tillade opheling af mundhulen.
Eosinofil øsofagitis er indberettet. I tilfælde af svær eller vedvarende gastro-øsofageale symptomer som dysfagi eller dyspepsi skal behandlingen afbrydes og der skal søge lægehjælp. Skal ordineres med forsigtighed til patienter med autoimmunsygdomme under remission. Interaktioner: Samtidig behandling med symptomlindrende medicin kan øge patientens toleranceniveau overfor immunterapi. Der skal tages højde for dette ved seponering af sådanne lægemidler. Graviditet og amning: Behandling bør ikke påbegyndes under graviditet. Der forventes ingen virkninger på børn, der ammes. Bivirkninger: Det kan forventes, at milde til moderate lokale allergiske reaktioner kan opstå inden for de første få dage, og at disse aftager igen ved fortsat behandling (1-3 måneder). For de fleste bivirkningers vedkommende kan reaktionen forventes at sætte ind inden for 5 minutter efter indtagelse og ophøre efter minutter til timer. Der kan forekomme mere alvorlige orofaryngeale allergiske reaktioner. Meget almindelige: Nasofaryngitis, ørepruritus, halsirritation, læbeødem, mundødem, oral pruritus. Almindelige: Bronkitis, faryngitis, rhinitis, sinusitis, dysgeusi, øjenpruritus, astma, hoste, dysfoni, dyspnø, orofaryngeale smerter, faryngealt ødem, mavesmerter, diarré, dysfagi, dyspepsi, gastroøsofageal reflux, glossodyni, glossitis, læbepruritus, mundsår, mundsmerter, tungepruritus, kvalme, oralt ubehag, erytem i mundslimhinden, oral paræstesi, stomatitis, tungeødem, opkastning, pruritus, urticaria, ubehag i brystet, træthed. Hvis patienten oplever signifikante bivirkninger af behandlingen, bør det overvejes at anvende symptomlindrende medicin.
Udlevering: B. Pakninger og priser: 30 frysetørrede sublinguale tabletter (Vnr 55 50 47),
90 frysetørrede sublinguale tabletter (Vnr 18 67 48). Dagsaktuelle priser findes på www.medicinpriser.dk.Tilskud: Generelt klausuleret tilskud. Indehaver af markedsføringstilladelsen: ALK-Abelló A/S. Repræsentant: ALK-Abelló Nordic A/S, Bøge Allé 6-8, 2970 Hørsholm, tlf. 38 16 70 70.
Produktinformation er forkortet i henhold til det godkendte produktresumé
29. januar 2024. Det fulde produktresumé kan vederlagsfrit rekvireres fra ALK-Abelló Nordic A/S.
GRAZAX® PHLEUM PRATENSE. Standardiseret allergenekstrakt af græspollen fra engrottehale. Frysetørrede sublinguale tabletter 75.000 SQ-T. Indikation: Sygdomsmodificerende behandling af græspolleninduceret rhinitis og conjunctivitis hos voksne og børn fra fem år, med klinisk relevante symptomer og diagnosticeret med en positiv hudpriktest og/eller specifik IgE test overfor græspollen. Dosering: En frysetørret sublingual tablet dagligt. Behandling med Grazax bør kun initieres af læger med erfaring indenfor behandling af allergiske sygdomme og mulighed for behandling af allergiske reaktioner. Ved behandling af børn skal lægen have erfaring i behandling af allergiske sygdomme hos børn. Det anbefales, at den første frysetørrede sublinguale tablet tages under medicinsk tilsyn (20-30 minutter). I den første behandlingssæson opnås klinisk effekt, hvis behandlingen initieres mindst 4 måneder før den forventede start af græspollensæsonen og fortsættes igennem hele græspollensæsonen. Hvis behandlingen initieres 2-3 måneder før sæsonen, kan nogen effekt forventes. Anbefalet behandlingstid er 3 år. Kontraindikationer: Overfølsomhed over for hjælpestofferne. Malignitet eller systemiske sygdomme med påvirkning af immunsystemet. Inflammatoriske tilstande i mundhulen med svære symptomer. Ukontrollerbar eller svær astma (hos voksne: FEV1 < 70 %, hos børn: FEV1 < 80 % af forventet værdi efter passende farmakologisk behandling). Særlige advarsler og forsigtighedsregler: Svære systemiske allergiske reaktioner: I klinisk anvendelse har der været indberettet tilfælde af alvorlige anafylaktiske reaktioner; i visse tilfælde ved doser efter den initiale dosis. Medicinsk tilsyn ved behandlingens start er derfor en vigtig sikkerhedsforanstaltning. I tilfælde af svære systemiske reaktioner, angioødem, synkebesvær, vejrtrækningsbesvær, stemmeændring, hypotension eller tæthed i halsen skal en læge straks kontaktes. I disse tilfælde skal behandling ophøre permanent eller indtil lægen råder anderledes. Hvis patienter med samtidig astma oplever symptomer og tegn på forværring af astmaen, bør behandling ophøre, og lægen bør omgående konsulteres for at vurdere, om behandlingen skal fortsættes. Behandling af patienter, som tidligere har haft en systemisk reaktion på subkutan immunterapi med græspollen, skal nøje overvejes, da de kan have en højere risiko for at få en systemisk reaktion med Grazax. Svære anafylaktiske reaktioner kan behandles med adrenalin. Overvej derfor om patienten kan tåle adrenalin i tilfælde af, at der forekommer en svær systemisk allergisk reaktion. Patienter med hjertesygdomme kan have øget risiko for svære systemiske allergiske reaktioner. Lokale allergiske reaktioner: Milde eller moderate lokale allergiske reaktioner kan forventes under behandlingen. Hvis patienten oplever betydelige lokale bivirkninger under behandlingen, bør antiallergisk medicin overvejes. Orale tilstande: I tilfælde af mundkirurgi, inklusiv tandudtrækning og ved tab af mælketand hos børn, bør behandling med Grazax ophøre i 7 dage for at tillade heling af den orale kavitet. Astma: Er en kendt risikofaktor for svære systemiske allergiske reaktioner. Patienter med astma skal informeres om, at de straks skal søge lægehjælp, hvis deres astma pludselig forværres. Hos patienter med astma, som oplever en akut luftvejsinfektion, bør initiering af behandling udsættes, indtil infektionen er ovre. Eosinofil øsofagitis: Hos patienter med svær eller vedvarende gastroøsofageale symptomer bør seponering af behandlingen overvejes. Samtidig vaccination: Vaccination kan gives uden at afbryde Grazaxbehandlingen efter lægelig vurdering. Interaktioner: Samtidig behandling med symptomatiske, anti-allergiske præparater kan øge patientens toleranceniveau overfor immunterapi. Der foreligger begrænsede data på mulige risici i forbindelse med samtidig immunterapi med andre allergener under behandling med Grazax. Graviditet og amning: Behandling med Grazax bør ikke initieres under graviditet. Det forventes ingen påvirkninger af børn, som ammes. Bivirkninger: Milde til moderate lokale allergiske reaktioner kan forekomme tidligt i behandlingen, men disse er tilbøjelige til at aftage spontant inden for 1 til 7 dage. I de fleste tilfælde forventes reaktionen at starte inden for 5 minutter efter dagens indtagelse af Grazax og aftage efter minutter eller timer. Sværere lokale eller systemiske allergiske reaktioner kan forekomme. Meget almindelige: Øre-pruritus, halsirritation, oral pruritus, oralt ødem. Almindelige: Øjenpruritus, conjunctivitis, hævelse af øjne, nysen, hoste, halstørhed, dyspnø, orofaryngeale smerter, faryngealt ødem, rinoré, tæthed i halsen, nasal kløe, hævelse af læber, oralt ubehag, oral paræstesi, stomatitis, dysfagi, mavesmerter, diarré, dyspepsi, kvalme, opkastning, erytem i mundslimhinden, orale sår, orale smerter, læbekløe, pruritus, urticaria, udslæt, træthed, ubehag i brystet. Anti-allergimedicin bør overvejes ved signifikante bivirkninger. Børn: Generelt svarer bivirkningsprofilen for pædiatriske patienter behandlet med Grazax til den, der er observeret hos voksne. Følgende bivirkninger forekom med en højere frekvens hos børn: Almindelige: øjenirritation, øresmerter, faryngealt erytem og blærer i mundslimhinden. Ikke almindelige: hævelse af ører. Udlevering: B. Pakninger og priser: 30 frysetørrede sublinguale tabletter (Vnr 025425), 100 frysetørrede sublinguale tabletter (Vnr 025736). Dagsaktuelle priser findes på www.medicinpriser.dk.Tilskud: Generelt klausuleret tilskud. Registreringsindehaver: ALK-Abelló A/S, Bøge Allé 6-8, 2970 Hørsholm.
Produktinformation er forkortet i henhold til det godkendte produktresumé 24. marts 2023. Det fulde produktresumé kan vederlagsfrit rekvireres fra ALK-Abelló Nordic A/S, Bøge Allé 6-8, 2970 Hørsholm, tlf. 38 16 70 70.
ITULAZAX® BETULA VERRUCOSA. Standardiseret allergenekstrakt af pollen fra vortebirk. Frysetørrede sublinguale tabletter 12 SQ-Bet. Indikation: Voksne patienter til behandling af moderat til svær allergisk rhinitis og/eller konjunktivitis induceret af pollen fra den gruppe, der er homolog til birk[1]. Til patienter med en klinisk historie med symptomer trods brug af symptomlindrende medicin og en positiv test for sensibilisering over for et medlem af den gruppe, der er homolog til birk (hudpriktest og/eller specifik IgE). Dosering: Én frysetørret sublingual tablet dagligt. Det anbefales, at behandling indledes uden for pollensæsonen og fortsætter i træpollensæsonen. Den kliniske effekt i træpollensæsonen (den gruppe, der er homolog til birk) er påvist, når behandling indledes mindst 16 uger før den forventede start af træpollensæson (den gruppe, der er homolog til birk) og fortsættes i hele sæsonen. Internationale retningslinjer henviser til en behandlingsperiode på 3 år for at opnå sygdomsmodifikation. Hvis der ikke observeres forbedring i løbet af det første års behandling, er der ingen indikation for at fortsætte behandlingen. Behandling skal initieres af læger med erfaring i behandling af allergiske sygdomme. Den første tablet skal tages under lægeligt opsyn, og patienten skal overvåges i mindst en halv time, for at patient og læge i den forbindelse kan få lejlighed til at drøfte evt. bivirkninger og mulig behandling deraf. Hvis behandlingen afbrydes i mere end 7 dage, anbefales det at kontakte en læge, før behandlingen genoptages.
Kontraindikationer: Overfølsomhed over for hjælpestofferne. FEV1 <70 % af den forventede værdi (efter tilstrækkelig farmakologisk behandling) ved initiering af behandlingen. Svær astma-eksacerbation inden for de seneste 3 måneder før initiering. Ikke-kontrolleret astma inden for de seneste 3 måneder før initiering. Aktive systemiske autoimmune sygdomme (responderer ikke på behandling) og immundefekter, nedsat immunforsvar eller immunosuppression. Malign neoplasia med aktuel sygdomsrelevans. Akut svær oral inflammation eller orale sår. Særlige advarsler og forsigtighedsregler: Svære systemiske allergiske reaktioner: Behandlingen skal seponeres, og en læge skal omgående kontaktes i tilfælde af svære systemiske allergiske reaktioner, svære astma-eksacerbationer, svært faryngealt ødem, synkebesvær, åndedrætsbesvær, stemmeforandringer, hypotension eller følelse af opfyldning i halsen. De indsættende systemiske symptomer kan omfatte rødmen, pruritus, varmefornemmelser, generelt ubehag og uro/angst. En mulig behandling af svære systemiske allergiske reaktioner er adrenalin. Virkningerne af adrenalin kan forstærkes hos patienter, der behandles med tricykliske antidepressiva, MAO-hæmmere og/eller COMT-hæmmere med mulige fatale følger. Virkningerne af adrenalin kan reduceres hos patienter, der behandles med betablokkere. Patienter med hjertesygdomme kan være udsat for øget risiko i tilfælde af svære systemiske allergiske reaktioner. Initiering hos patienter, der tidligere har haft en systemisk allergisk reaktion over for subkutan træpollenallergen-immunterapi, skal nøje overvejes, og der skal være foranstaltninger til rådighed til behandling af mulige reaktioner. Astma: Er en kendt risikofaktor for svære systemiske allergiske reaktioner. Svær astma-eksacerbation inden for de seneste 12 måneder er en kendt risikofaktor for fremtidige eksacerbationer. Patienter med astma skal informeres om, at de skal søge lægehjælp omgående, hvis deres astma pludselig forværres. Hos patienter med astma, som oplever en akut luftvejsinfektion, bør initiering af behandling med Itulazax udsættes, indtil infektionen er ovre. Oral inflammation: Hos patienter med svær oral inflammation, orale sår eller efter oral kirurgi, herunder dental ekstraktion eller efter tab af tand, bør initiering af behandling med Itulazax udskydes, og igangværende behandling midlertidigt seponeres for at tillade opheling af mundhulen. Lokale allergiske reaktioner: Kan forventes i behandlingsperioden. Disse er i reglen milde til moderate, men der kan forekomme mere alvorlige reaktioner. De første par dage med behandling i hjemmet kan der forekomme bivirkninger, som ikke blev observeret på den første behandlingsdag. Hvis patienten oplever signifikante lokale bivirkninger af behandlingen, bør anti-allergisk medicin (f.eks. antihistaminer) overvejes. Eosinofil øsofagitis: Er indberettet. Hos patienter med svær eller vedvarende gastro-øsofageale symptomer skal behandlingen afbrydes, og der skal søges lægehjælp. Autoimmune sygdomme under remission: Ordineres med forsigtighed. Samtidig vaccination: Vaccination kan gives uden at afbryde behandlingen med Itulazax efter lægelig vurdering af patientens almentilstand. Interaktioner: Samtidig behandling med symptomlindrende anti-allergisk medicin kan øge patientens toleranceniveau over for immunterapi. Der skal tages højde for dette ved seponering af sådanne lægemidler. Graviditet og amning: Behandling bør ikke påbegyndes under graviditet. Der forventes ingen virkninger på børn, der ammes. Bivirkninger: Milde til moderate lokale allergiske reaktioner kan opstå inden for de første få dage, og at disse aftager igen inden for få måneder (i mange tilfælde inden for 1-2 uger). For de fleste bivirkningers vedkommende kan reaktionen forventes at sætte ind inden for 10 minutter efter indtagelse af Itulazax efter hver daglig indtagelse og ophøre inden for en time. Der kan forekomme mere alvorlige lokale allergiske reaktioner. Meget almindelige: Ørepruritus, halsirritation, mundødem, oral pruritus, oral paræstesi, tungepruritus. Almindelige: Rhinitis, oralt allergisyndrom, dysgeusi, symptomer på allergisk konjunktivitis, hoste, halstørhed, dysfoni, dyspnø, orofaryngeal smerte, faryngealt ødem, faryngeal paræstesi, mavesmerte, diarré, dyspepsi, dysfagi, gastroøsofageal reflukssygdom, glossodyni, oral hypæstesi, læbeødem, læbepruritus, kvalme, oralt ubehag, blærer i mundslimhinden, stomatitis, hævet tunge, urticaria, ubehag i brystet, følelse af fremmedlegeme.
Udlevering: B. Pakninger og priser: 30 frysetørrede sublinguale tabletter (Vnr 08 13 44), 90 frysetørrede sublinguale tabletter (Vnr 46 25 44). Dagsaktuelle priser findes på www.medicinpriser.dk. Tilskud: Generelt klausuleret tilskud. Indehaver af markedsføringstilladelsen: ALK-Abelló A/S. Repræsentant: ALK-Abelló Nordic A/S, Bøge Allé 6-8, 2970 Hørsholm, tlf. 38 16 70 70.
Produktinformation er forkortet i henhold til det godkendte produktresumé
18. oktober 2023. Det fulde produktresumé kan vederlagsfrit rekvireres fra ALK-Abelló Nordic A/S.